丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂婓搚椶嬥懏偺幚尡
丂丂乮侾乯丂婓搚椶尦慺偲偦偺怓丗
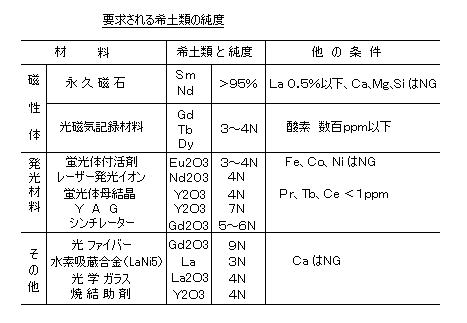
丂丂婓搚椶尦慺乮儗傾丒傾乕僗乯偼丄乭婬乮傑傟乯側搚椶嬥懏尦慺乮俙倢丄俧倎丄俬値側偳乯乭偱偼側偔丄寢峔側検偑抧妅傗塅拡偵峀偔暘晍偟偰偄傞丅乮塅拡懚嵼搙乮僗儁僋僩儖娤應偐傜偺梊應抣乯偱偼丄俽倰丗俀俁丏俆丄俛倎丗係丏係俋丄俼倐丗俈丏侽俋丄俠倱丗侽丏俁俈俀 偩偐傜丄偙傟傜偵旵揋偡傞丅傑偨丄抧妅偵偍偗傞懚嵼搙偱偼丄嵟傕彮側偄俿倣乮僣儕僂儉乯偱偝偊侽丏俀倫倫倣偱丄價僗儅僗偲摨掱搙偱偁傝丄嬥丄敀嬥偺侽丏侽侽俆倫倫倣傛傝傕偼傞偐偵懡偄丅
丂丂婓搚椶尦慺偺帒尮偼崱屻侾俀侽侽擭偼嵦孈偱偒傞偲偄傢傟傞傎偳懡偄偑丄僀僆儞偺奜妅揹巕偑摨偠峔憿偺偨傔丄帡偨傛偆側壔妛揑惈幙乮壙悢偼庡偵亄俁壙偱丄傾儖僇儕搚椶嬥懏乮俵倗丄俠倎側偳乯偵嬤偄惈幙乯傪帩偮偺偱丄憡屳偺暘棧丒惛惢偑旕忢偵擄偟偔丄弮昳偑 倠倗扨埵傗僩儞扨埵偱惗嶻偝傟傞傛偆偵側偭偨偺偼丄乭梟攠拪弌朄乮仏乯乭偑妋棫偟偨愴屻乮侾俋俇侽擭戙埲崀乯偺偙偲偱偁傞丅
丂丂丂丂仏丂拪弌嵻偲偟偰 倓倝乮俀-僄僠儖僿僉僔儖乯椨巁乮俢俀俤俫俹俙乯丄椨巁僩儕僽僠儖乮俿俛俹乯丄俀-僄僠儖僿僉僔儖椨巁-儌僲俀-僄僠儖僿僉僔儖僄僗僥儖乮俤俫俤俫俹俙乯側偳傪梟偐偟崬傫偩働儘僔儞傗値-僿僾僞儞傪梡偄偰丄婓搚椶傪梟偐偟崬傫偩悈梟塼憌偲怳偲偆偡傞偲丄廳婓搚傎偳嶖懱偺埨掕搙偑崅偄偺偱偙偺梟攠懁偵拪弌偝傟傞丅乭岦棳懡抜憰抲乭偵傛偭偰楢懕揑偵悢廫抜拪弌憖嶌傪峴側偆丅
丂丂婓搚椶尦慺偼尨巕斣崋偑戝偒偔側傞偵廬偭偰丄捠忢偺尦慺偲偼堎側傞揹巕偺媗傑傝曽偑側偝傟傞丅俆俈斣乮儔儞僞儞乯乣俈侾斣乮儖僥僠僂儉乯偺堦楢偺尦慺孮乮儔儞僞僲僀僪乯偺丄奜妅偺揹巕偺屄悢偑曄傢傜偢丄撪懁偺 係倖 婳摴偺揹巕偑 侽屄乣侾係屄傑偱堦偮偢偮憹偊偰偄偔丅偙傟偵廬偭偰丄枾搙丄僀僆儞敿宎丄梈揰側偳偑曄壔偟丄廳婓搚傎偳廂弅偟偰偄偔丅乮儔儞僞僲僀僪廂弅乯丂偙偺 係倖 婳摴揹巕偙偦偑丄婓搚椶尦慺偺惈幙傪摿挜晅偗傞尨場偱偁傞丅乮仏丂俹倣偼曻幩惈偱僨乕僞偑彮側偄乯
丂丂儔儞僞僲僀僪偺亄俁壙僀僆儞偼丄俆倱2丄俆倫6 偺婳摴偑枮攖偱丄偦偺撪懁偺係倖 婳摴揹巕偑尨巕斣崋偵廬偭偰堦偮偢偮憹偊偰偄偔丅廬偭偰丄婓搚椶摿桳偺偒傢傔偰桳梡側怓傗寀岝丄帴婥揑丄揹婥揑丄岝妛揑側惈幙偼丄偙偺係倖 婳摴揹巕偺怳傞晳偄偑丄俆倱2丄俆倫6 偺奜妅揹巕偵傛偭偰庣傜傟丄奜晹偲偺寢崌嬶崌偵傎偲傫偳塭嬁偝傟側偄偙偲偵傛偭偰敪尰偝傟傞丅
丂丂偟偨偑偭偰丄旕忢偵塻偄寀岝僗儁僋僩儖傪傕偮寀岝懱乮俿倁丄俠俼俿丄倃慄丄寀岝摂梡乯傗偙傟傪棙梡偟偨俶倓-倄俙俧儗乕僓乕丄柍婡暔偲摨條偵敪岝偡傞桳婡嶖懱偺寀岝懱丄帴婥儌乕儊儞僩偑懪偪徚偟崌傢側偄偱寢徎峔憿偵屌掕偝傟傞偙偲偵傛傞嫮椡側 僒儅僐僶丄僱僆僕儉帴愇丄岝帴婥婰榐攠懱偲偟偰丄傑偨丄掅懝幐偺岝僼傽僀僶乕丄摟柧嫮帴惈懱偺傾僀僜儗乕僞乕乮倄俬俧丄俧俧俧乯丄揹榗慺巕側偳偺尰戙偺偝傑偞傑側僴僀僥僋婡婍偵梡偄傜傟偰偄傞丅
丂丂傑偨丄係倖 婳摴揹巕偵娭學側偄偑丄巁壔暔崅壏挻揱摫懱乮倄丄俴倎乯丄崅孅愜棪丒崅暘嶶偺岝妛僈儔僗乮俴倎乯丄揝峾惛楤偺揧壛嵻乮儈僢僔儏儊僞儖乯丄堛栻昳側偳丄偝傑偞傑側梡搑偑偁傞丅

丂丂丒丂婓搚椶嬥懏偼柍悈墫壔暔傪梟梈揹夝偟偰嶌傜傟傞丅丂嬥懏偼挿偄娫嬻婥拞偵曻抲偟偰偍偔偲昞柺偑巁壔偡傞丅傑偨婓搚椶嬥懏丄巁壔暔丄扽巁墫偼丄墫巁側偳偺峼巁偵梕堈偵梟偗丄偦傟偧傟偺墫偺梟塼偲側傞丅丂懠偺婓搚椶偑暘棧偝傟偰偄側偄僙儕僂儉乮儔儞僞儞側偳偺晄弮暔傪懡偔娷傓乯偼乭儈僢僔儏儊僞儖乭偲屇偽傟丄揝偲偺崌嬥乮俠倕側偳丗俉侽亾丄俥倕俀侽亾乯偲偟偰丄儔僀僞乕偺敪壩愇偵梡偄傜傟傞丅傑偨儔儞僞儞傗僙儕僂儉偺巁壔暔乮俴倎2俷3丄俠倕俷2乯偼梈揰偑崅偔丄墛偱擬偡傞偲敀擬偟偦偺岝婸偑嫮偄偙偲偐傜丄僩儕僂儉偺巁壔暔乮俿倛俷2乯偲崿偤偰奨楬徠柧梡偺僈僗儅儞僩儖偲偟偰梡偄傜傟偨丅 僙儕僂儉偺巁壔暔乮僙儕傾丄俠倕俷2乯偼丄僈儔僗偺尋杹嵻偲偟偰梡偄傜傟傞丅
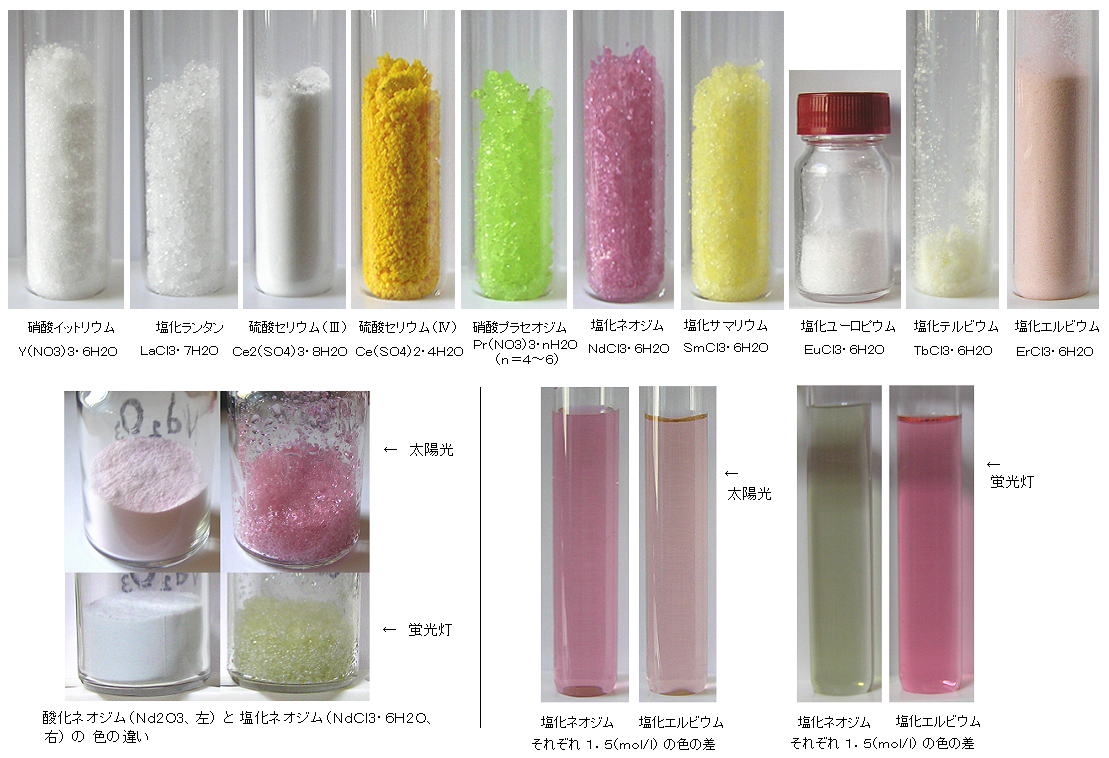
丂丂丒丂扨懱嬥懏偺怓偼偡傋偰嬧敀怓偱偁傞偑丄僀僆儞偲側傞偲拝怓偡傞傕偺偑懡偄丅偙偺怓偼丄係倖 婳摴偺晄懳揹巕偺屄悢偲枾愙側娭學偵偁傞丅乮偨偲偊偽丄俤倰亄3丗 仾伀丄仾伀丄仾伀丄仾伀丄仾丂丄仾丂丄仾丂 偱丄晄懳揹巕偼俁屄偱偁傝丄摨偠俁屄偺 俶倓亄3偲摨宯摑偺怓乮僺儞僋乣巼乯丅 僄儖價僂儉僀僆儞偼摨偠婳摴撪偺懳揹巕偵傛傝幷暳偝傟丄摨偠擹搙偺僱僆僕儉僀僆儞悈梟塼傛傝傕怓偑撥偭偰偄傞丅 僣儕僂儉乮俿倣亄3乯偼偝傜偵敄偄椢丅丂晄懳揹巕偼 俧倓偺7屄偑嵟戝乯
丂丂丒丂婓搚椶尦慺偺僀僆儞偼丄庡偵亄俁壙偺壙悢傪傕偮丅乮仏丂偨偩偟丄俠倕偼俁壙偲係壙丄俤倳偼俀壙偲俁壙傪傕偮丅巁壔暔偼傕偭偲暋嶨偱丄俼2俷3 偺婎杮宍偺懠偵丄俠倕俷2乮敄偄烌乯丄俹倰6俷11乮崟乯丄俿倐4俷7乮妼怓乯丄傾僋僠僲僀僪偺僂儔儞傕 倀俷2丄倀3俷8乯丂婓搚椶僀僆儞偺怓偼丄摵傗揝側偳偺懠偺慗堏尦慺偺僀僆儞偺怓偲堎側傝丄晛捠偺幨恀偱嶣傞偲怓崌偄偑栚帇偲堎側偭偰幨傞偙偲偑懡偄丅丂僱僆僕儉僀僆儞偼丄懢梲岝偲揹摂岝偱偼愒巼丄寀岝摂偱偼惵怓偵尒偊傞丅乮乭僱僆僕儉僈儔僗乭傕摨偠乯丂傑偨丄儐乕儘僺僂儉墫偼柍怓偱偁傞偑丄巼奜慄偑崿偠傞偲寀岝偺偨傔愒枴傪懷傃傞丅儐乕儘僺僂儉丄僥儖價僂儉側偳偼丄懠偺婓搚椶巁壔暔傗儕儞巁墫側偳偵僪乕僺儞僌偝傟丄俿倁丄俠俼俿丄寀岝摂丄敄枌俤俴側偳偺寀岝懱偲偟偰梡偄傜傟傞丅丂巁壔僾儔僙僆僕儉偼缰栻乮僾儔僙僆僕儉墿丗 僕儖僐儞丗 倅倰俽倝俷4 偺 倅倰 傪 俹倰4亄偱堦晹抲姺偟偨傕偺乯偵梡偄傜傟傞丅
丂丂



丂丂乮俀乯丂婓搚椶偺寀岝懱丗
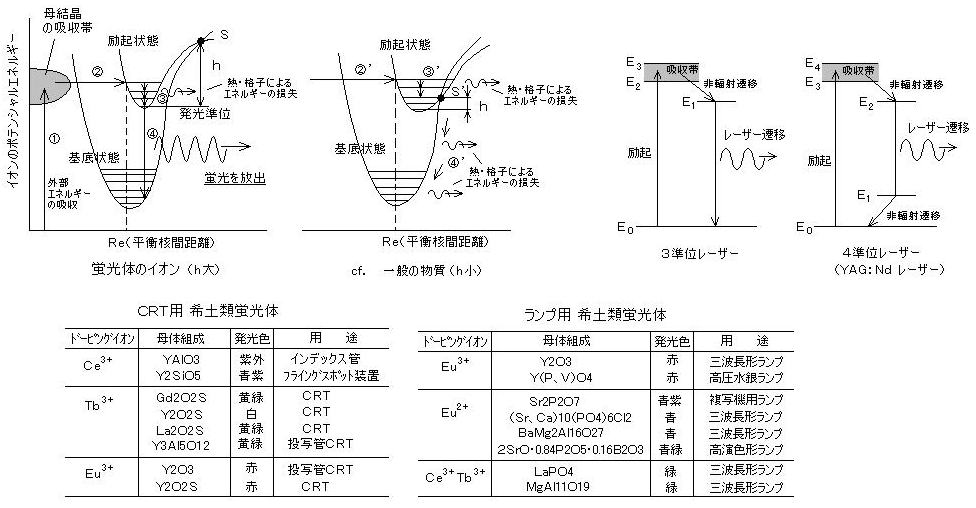
丂丂係倖 婳摴揹巕偼奜晹偺塭嬁傪庴偗偵偔偄偺偱丄 係倖 - 係倖 慗堏傪偡傞 俹倰3+丄俶倓3+丄俽倣3+丄俤倳3+丄俧倓3+丄俿倐3+丄俢倷3+丄俫倧3+丄俤倰3+丄俿倣3+丄倄倐3+ 偼丄僗儁僋僩儖偑塻偄僺乕僋偺寀岝傪敪偡傞丅 偙傟偼丄俶倓-倄俙俧儗乕僓乕丄俿倁丒俠俼俿偺僽儔僂儞娗丄崅墘怓惈偺寀岝儔儞僾丄俤俴敪岝懱側偳偵梡偄傜傟傞丅 堦曽丄 係倖 - 俆倓 慗堏傪偡傞 俠倕3+丄俤倳2+丄倄倐2+ 偱偼丄傛傝暆峀偄僗儁僋僩儖傪梌偊傞丅乮伀 昞乯
丂丂丒丂墫壔儐乕儘僺僂儉偺價儞偵捈愙丄嬤巼奜慄 俴俤俢乮兩佮係侽侽値倣乯偺岝傪摉偰傞偲丄俤倳3+摿桳偺愒怓偺寀岝乮兩亖俇侾俆値倣乯傪敪偡傞丅乮仺乯
丂丂僪乕僺儞僌偡傞曣寢徎偼丄僀僆儞敿宎偑摨偠掱搙偱媧廂懷偑僀僆儞偺椼婲忬懺傛傝傕崅偄偲偄偆娭學傪枮偨偡丅偙偺曣寢徎偵僪乕僺儞僌偝傟偨婓搚椶僀僆儞偺寀岝偼丄
丂丂嘆丂傛傝僄僱儖僊乕偺崅偄乮攇挿偺抁偄乯岝偵傛偭偰丄曣寢徎偵媧廂偝傟偨僄僱儖僊乕偑丄嘇 婓搚椶偺敪岝僀僆儞偵揱傢傝丄僀僆儞偑崅偄僄僱儖僊乕弴埵偵椼婲偝傟丄嘊 敪岝弴埵偵払偟偰偐傜丄嘋 婎掙忬懺偵棊偪傞帪偵丄偦偺摿桳偺攇挿偺岝傪曻弌偡傞偙偲偵傛偭偰婲偙傞丅 寀岝暔幙偼丄乮伀 嵍恾乯乯偺 倛 偑戝偒偄偺偱丄擬丒奿巕怳摦偵傛傞懝幐暘偑彫偝偔丄敪岝岠棪偑崅偄丅乮 們倖丏 倛 偑彫偝偄堦斒偺暔幙偱偼丄椼婲忬懺偲婎掙忬懺偺岎揰俽傪捠偭偰丄偡傋偰擬丒怳摦偲偟偰僄僱儖僊乕傪幐偭偰偟傑偆丅乯
丂丂仏丂戙昞揑側屌懱儗乕僓乕偺 俶倓-倄俙俧乮倄3俙倢5俷11丗俶倓3亄乯儗乕僓乕偼丄係弨埵儗乕僓乕偱丄儗乕僓乕慗堏弨埵偺廔弨埵偑丄俁弨埵儗乕僓乕乮儖價乕丒儗乕僓乕側偳乯傛傝傕崅偄埵抲偵偁傞偨傔丄庛偄椼婲偱乭斀揮暘晍乭乮亖婎掙揹巕傛傝傕椼婲揹巕偺悢偺傎偆懡偄忬懺偱丄僐僸乕儗儞僩側敪怳偵昁梫乯傪宍惉偱偒丄楢懕敪怳傕梕堈偱偁傞丅偨偩偟丄懠偺僀僆儞偑崿嵼偡傞偙偲偵傛傞備傜偓偵傛傞桿摫曻弌偺塭嬁傪旔偗傞偨傔丄儗乕僓乕梡曣寢徎偺嵽椏偵偼崅弮搙乮俈俶乯偑梫媮偝傟傞丅乮伀 塃恾乯
丂
丂丂丒丂寀岝懱偺崌惉幚尡丗丂丂捠忢偼丄僀僢僩儕僂儉墫偵捑揳嵻偲偟偰溟巁 乮俠俷俷俫乯2 傪梡偄丄溟巁墫偲偟偰捑揳偝偣乮婓搚椶墫偼 俆亾傑偱偺墫巁巁惈偱傕丄掕検暘愅偑偱偒傞傎偳姰慡偵捑揳偡傞丅偙傟偼丄婓搚椶嬥懏偲懠偺傾儖僇儕搚椶嬥懏側偳偲偺暘棧偵梡偄傜傟傞乯丄偙傟傪鄅夁丄壛擬偟偰巁壔暔偵偟偰偐傜丄梈嵻偲偟偰侾亾掱搙偺儂僂巁僶儕僂儉傪崿崌偟偰侾俀侽侽亷亊係侽倛倰傎偳嫮擬偟偰寢徎棻傪俆乣俇兪倣偵惉挿偝偣偰嶌惢偡傞丅梈嵻偑柍偄偲侾係侽侽亷偱傕從惉偑姰椆偟側偄丅
丂丂偙偙偱偼丄徤巁僀僢僩儕僂儉乮倄乮俶俷3乯3丒俇俫2俷丄俋俋丏俋亾乮亖俁俶乯乯偵丄偦偺乮嬥懏姺嶼偱乯俆乣俇亾偺墫壔儐乕儘僺僂儉乮俤倳俠倢3丒俇俫2俷丄俋俋丏俋亾乯傪壛偊弮悈乮扙僀僆儞悈乯偵梟偐偟丄傾儞儌僯傾悈偱悈巁壔暔偲偟偰嫟捑偝偣傞丅捑揳偟偨悈巁壔暔偼旕忢偵嵶偐偔丄僎儖忬偵側偭偰偄傞偺偱丄鄅夁丒愻忩偼偟偵偔偄偑丄從惉偼偟傗偡偄丅捑揳偼弮悈偱侾夞偱愻偆丅乮巆偭偰偄傞傾儞儌僯傾側偳偼從惉偵傛偭偰婗嶶偡傞乯丂從惉偺嵺丄梈嵻偼揧壛偣偢丄偦偺傑傑 抐擬惈偺椙偄傾儖儈僫僙儔儈僢僋丒僔乕僩忋偵揾偭偰丄僴儞僪僶乕僫乕偺嵟嫮壩椡偱從偔偲丄寀岝懱偑抁帪娫偱從惉偱偒傞丅丂乮 拲乯 帋栻偵偼崅弮搙昳傪梡偄傞傋偒偱偁傝丄椨巁儔儞僞儞嶌惉梡偺墫壔儔儞僞儞偵俋俆亾昳傪梡偄偨帪偼岝傜側偐偭偨乯丂偙偺寀岝懱偼曣寢徎拞偵僪乕僺儞僌偝傟偰偄偰丄曣寢徎乮倄2俷3乯傪傑偢椼婲偡傞昁梫偑偁傞偺偱丄嬤巼奜慄乮巼奜慄俴俤俢乮係侽侽値倣乯傗僽儔僢僋儔僀僩乯偱偼慡偔岝傜偢丄兩亖俀俆俁丏俈値倣偺嶦嬠摂偺巼奜慄偵傛傞椼婲偱柧傞偄愒怓偺寀岝傪敪偡傞丅
丂丂

丂丂乮俁乯丂婓搚椶偺帴惈丗
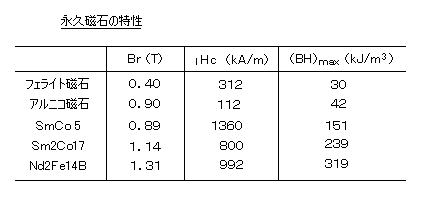
丂丂婓搚椶偺帴惈傕丄偙偺係倖 婳摴揹巕偑廳梫側栶妱傪壥偨偟偰偄傞丅丂塱媣帴愇偺惈擻偼丄俛亅俫嬋慄忋偱偺俛偲俫偺愊偺嵟戝抣乮乮俛俫乯倣倎倶乯偱寛傑傞丅嫮偄帴愇傪嶌傞偨傔偵偼丄巆棷帴懇枾搙 俛倰乮帴応傪庢傝嫀偭偨偲偒偵巆傞帺敪帴応乯偩偗偱側偔丄曐帴椡 俫們乮媡岦偒偺帴応偵懳偡傞掞峈椡乯傕僶儔儞僗傛偔忋偘側偗傟偽側傜側偄丅丂俁倓尦慺偺帴惈偺扴偄庤偼俁倓揹巕偱偁傝丄嵟奜妅側偺偱傎偲傫偳婳摴塣摦偼幐傢傟偰偟傑偆丅堦曽丄婓搚椶偱偼丄奜晹偺塭嬁傪庴偗側偄 撪懁偺係倖 揹巕偑丄寢徎偺拞偱嵟傕僄僱儖僊乕偑彫偝偔側傞傛偆偵曽岦偑屌掕偝傟傞丅偟偨偑偭偰丄俁倓尦慺乮揝傗僐僶儖僩側偳乯偲偺崌嬥偺応崌丄傑偢婓搚椶尨巕偺帴婥儌乕儊儞僩偑屌掕偝傟丄師偵丄岎姺憡屳嶌梡偵傛偭偰寢傃晅偗傜傟偰偄傞俁倓慗堏尦慺偺儌乕儊儞僩偺岦偒傕屌掕偝傟丄寢嬊丄寢徎慡懱偺帴壔偺岦偒偑嫮椡側乭堦幉堎曽惈乭傪敪尰偡傞傛偆偵屌掕偝傟傞丅僒儅僐僶丄僱僆僕儉帴愇偱偼丄偙偺曐帴椡 俫們偑奿抜偵戝偒偄偺偱丄崅偄乮俛俫乯倣倎倶 偑幚尰偡傞丅
丂丂傑偨丄婓搚椶帴愇偱偼丄寢徎棻撪偱帴暻堏摦偟傗偡偔 帴壔斀揮偑梕堈偵婲偙傞偺偱丄旝嵶側暡枛傪從寢偡傞曽朄乮暡枛栬嬥乯偑嵦傜傟偰偄傞丅帴愇梡偺婓搚椶偺弮搙偼丄埲忋偺棟桼偵傛傝丄俋俆亾埲忋偱偁傟偽椙偄丅
丂丂僱僆僕儉帴愇偼丄壏搙偑忋徃偡傞偵偮傟 俛倰丄俫們嫟媫懍偵掅壓偡傞寚揰偑偁傞乮俿們乮僉儏儕乕壏搙乯俁侾侽亷丄偨偩偟幚梡懴擬壏搙偼栺俉侽亷乯乯偺偱丄彫宆丒惛枾婡夿側偳偺巊梡暘栰偵傛偭偰偼崅壏偵嫮偄僒儅僐僶偑暪梡偝傟偰偄傞丅 僱僆僕儉帴愇偼僱僆僕儉偺堦晹傪僕僗僾儘僔僂儉乮俢倷乯偱抲姺偡傞偙偲偵傛傝崅壏偱巊梡壜擻乮侾亾揧壛偱侾俆亷夵慞乯偲側傝丄僴僀僽儕僢僪僇乕側偳偱懡検偵梡偄傜傟偰偄傞丅乮仏丂偨偩偟丄婓搚椶丄摿偵偙偺僕僗僾儘僔僂儉偼嶻弌偑曃偭偰偄傞乮拞崙丒撪儌儞僑儖偺晽壔壴浖娾乯偺偱丄擔杮偼埨掕妋曐偺偨傔僇僓僼僗僞儞丄儀僩僫儉側偳偺嫟摨奐敪傪恑傔偰偄傞丅乯丂傑偨丄僱僆僕儉帴愇偼嶬傃傗偡偄偺偱僯僢働儖側偳偺傔偭偒偑巤偝傟偰梡偄傜傟偰偄傞丅
丂丂丒丂悈偵晜偐傋偨侾墌嬍偵僱僆僕儉帴愇傪嬤偯偗傞偲丄傾儖儈僯僂儉偼斀帴惈側偺偱斀敪偟偰棧傟偰偄偔丅 僈僪儕僯僂儉傗僥儖價僂儉偼僉儏儕乕壏搙俿們偑掅偄偵傕偐偐傢傜偢丄僱僆僕儉帴愇偺傛偆側嫮椡側帴愇傪嬤偯偗傞偲帴壔偟偰忢壏偱傕媧偄晅偔丅壏搙傪忋偘傞偲億儘儕偲棊偪傞丅
丂丂丒丂僉儏儕乕壏搙 俿們乮嫮帴惈揮堏壏搙 俿俶乯偺應掕丗丂乮庛帴応偱乯壏搙偑忋徃偟偰帴惈傪幐偆壏搙偼 僉儏儕乕壏搙乮俿們乯偲屇偽傟丄扨懱嬥懏偺僈僪儕僯僂儉乮俧倓乯偱偼侾俆亷丄僥儖價僂儉乮俿倐乯偱偼亅俆俀亷側偺偱偙傟傪應掕偡傞丅帋椏偼丄敄枌僗僷僢僞儕儞僌梡僞乕僎僢僩乮俋俋丏俋亾丄冇侾俆倣倣亊倛俆倣倣乯偵冇俇倣倣偺寠傪奐偗偨僩乕儔僗傪梡偄偨丅
丂丂丂乮乮嶲峫乯丗俴儊乕僞偺夞楬乮廐寧揹巕偺僉僢僩乯乯
丂丂仏丂僈僪儕僯僂儉偼掅壏偱嫮帴惈懱偱偁傞偑丄僥儖價僂儉偼俿俶乮僱乕儖壏搙乯埲壓偱丄斀嫮帴惈偵暘椶偝傟傞 傜偣傫帴惈傪尰傢偟丄掅壏偱塃忋偑傝偺嬋慄偵側傞丅崅壏椞堟偱偼偳偪傜傕僉儏儕乕丒儚僀僗偺朄懃 冊亖俠/乮俿亅俿們乯 倧倰 冊亖俠/乮俿亅俿俶乯 偵嬤帡揑偵廬偆丅
